一、介绍
做为基因突变,癌症和衰老等症状的重要指标,DNA和染色体损伤越来越受到生物学界的关注。DNA损伤可以自发也可由离子照射,环境毒素或者化学毒素诱导产生。有许多种体外实验可以鉴定化合物的基因毒性及其作用机制。组蛋白H2AX丝氨酸139位点的磷酸化是DNA双链缺失的早期并且敏感的指标,另外在DNA损伤后肿瘤抑制蛋白53BP1也会磷酸化(通常伴随着DNA修复)并形成核内小点。
在本研究中我们发明了一种自动三色高通量成像技术用来评估化合物造成DNA损伤的程度,这项技术基于通过对组蛋白H2AX和53BP1磷酸化的免疫荧光检测,从而比较control组和经过丝裂霉素C(MMC)、过氧化氢或者依托泊苷处理过的细胞在DNA损伤上的差别。
二、可视化核内小点指示DNA损伤位置
利用ImageXpress Micro高内涵成像分析系统和商业购买的试剂,实验者可以完成多种细胞的DNA损伤可视化。
结合H2AX和53BP1的一抗可以被荧光标记的二抗检测到并结合,两者的荧光激发光/发射光范围分别为495/519和640/680 nm。为了准确检测到每个细胞核中的小点,在高倍率(至少40倍)的镜下采集到的图像才被用于分析,图像应用标准的FITC和Cy5通道拍摄。
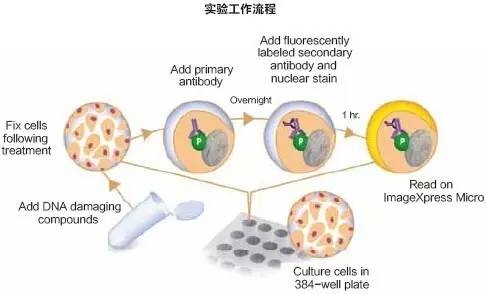
三、多参数DNA损伤实验的实验流程如下:
• 以每孔5000-7500的密度将细胞种到384孔黑壁薄底聚苯乙烯微孔板中
• U20S或者CHO细胞37度过夜培养
• 用不同稀释浓度的MMC或者依托泊苷处理细胞24h或者用过氧化氢处理2h
• 换培养基后让细胞37度下静置30min,4%多聚甲醛室温固定20min
• 用PBS清洗细胞终止固定,室温下穿孔细胞1h
• 加入抗H2AX和抗53BP1的一抗,4度过夜孵育
• 1*PBS洗3次
• 加入荧光标记的二抗,室温孵育1h
• 加入16uM Hoechst 33342核染料(终浓度),室温孵育15min
• 1*PBS洗3次
• 在3个通道下获取图像
• 进行图像分析
对DNA损伤可以用由易到难得三种方法进行定量,具体方法在下一部分进行阐述。
四、利用简单细胞分类分析方法鉴定损伤的细胞核
预制MetaXpress®软件的分析模块——细胞分类,可以根据DNA损伤标记对细胞核进行阳性和阴性的分类,可以直接得到含有阳性标记的细胞百分比。宽场模式10倍物镜条件下对每孔进行单视野成像,可以快速成像并进行相应的分析。即便最高浓度的化合物单视野下也可以捕获超过500个细胞,而在MMC毒性浓度以下则每个视野可以捕获超过2800个细胞。

五、利用共聚焦成像提高单一核内小点计数的准确性
多种参数例如数量、平均密度、总面积、每个细胞或者每孔的总密度都可以用来统计染色的核内小点。在这个实验中,我们利用ImageXpress Micro共聚焦成像分析系统在宽场模式或者60um针孔共聚焦模式下在每个孔都获取了多个图像。两种模式都用40x平场复消色差物镜拍摄。利用MetaXpress软件简单的用户自定义模块对细胞核内特异性的小点进行计数。由于共聚焦成像可以屏蔽掉板外物体的荧光,所以核内小体显示的非常清晰并且容易区分。我们的实验结果显示利用共聚焦模式可以对核内小体更准确的计数,从而在更广的动态区间内(信号/背景)和更高的Z’ factor下得到更可靠的结果。

六、两种标记共定位的测量
用两种不同的DNA损伤标记进行共定位可以让我们更方便的了解化合物对细胞核损伤的机制。使用用户自定义模块对高倍物镜共聚焦图像进行分析,包括对DNA损伤修复蛋白53BP1和之前介绍的双链DNA损伤标记(H2AX阳性细胞百分比,每个细胞核小点计数/密度/面积),从而得到相应细胞的共定位标记值。
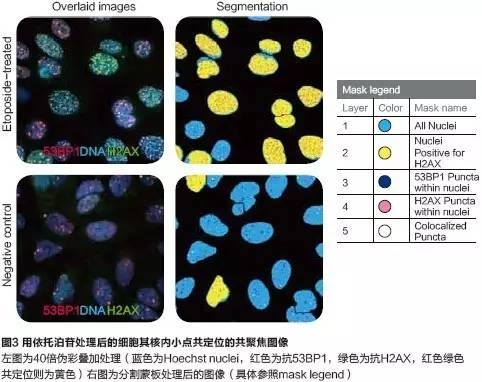
总结
我们展示了运用ImageXpress Micro共聚焦或宽场成像模式对H2AX和53BP1进行灵敏多参数检测的实验,提供了一个可以高通量筛选DNA损伤并进行定量计算的方法。传统上,共聚焦用于精确识别与核染色共定位的核内小点。在我们的实验中,宽场成像模式下分析结果的z’ factors只有不到0.5,而共聚焦成像模式下的实验稳定性却很好。另外,可以多荧光标记同时使用同时分析的能力,可以最大限度上节约细胞、试剂和时间。
更多详情请关注Molecular Devices美谷分子仪器官网
推荐阅读:莱芜信息港

